MS, Alzheimer gibi beyin hastalıklarında kan-beyin bariyeri aşıldı
 Alzheimer ve beyin kanserlerinde ilaçlar artık daha etkili olabilecek
Alzheimer ve beyin kanserlerinde ilaçlar artık daha etkili olabilecek
Cornell Üniversitesi araştırmacıları, bin yıllık bilmeceyi nihayet çözmeyi başardı. Bilim adamları, kan-beyin bariyerini güvenli bir şekilde aşarak, Alzheimer hastalığı, multipl skleroz ve merkezi sinir sistemi kanserlerinin tedavisinde ilaçların etkili bir şekilde tutulumlu bölgelere ulaşmasını sağladı. Çalışmadan elde edilen verilerle birlikte MS, Alzheimer ve beyin kanserlerinde ilaçlar artık daha etkili olabilecek. Çalışma ayrıca yeni ilaçların geliştirilmesi konusunda da önemli katkılar sunuyor.
Çalışmanın araştırmacıları, vücut tarafından üretilen adenozin molekülünün beyne ulaşması gereken büyük molekülleri modifiye ettiğini keşfetti. İlk kez bu çalışmada adenozin reseptörlerinin kan-beyin bariyeri hücrelerinde aktifleştiğinde, bariyerin aşılabileceği belirlendi. Çalışmayı fareler üzerinde yapan araştırmacılar, bu bulgunun insan hücrelerinde de aynı sonuçları verdiğini gördü. Ayrıca araştırmacılar, FDA tarafından onaylanmış ve durumu kritik hastalarda kalbin görüntülenmesinde kullanılan Lexiscan adlı adenozin bazlı ilacın da kan-bariyerini aşabildiğini buldu.
Kan-beyin bariyeri, beyindeki kan damarlarını oluşturan özel hücrelerden oluşur. Bu bariyer sayesinde, vücuda giren maddeler kana karışamaz ve beyne ulaşmaz. Bu bariyerden yalnızca amino asit, oksijen, glukoz ve su gibi hayati moleküller geçebilir. Bariyer o kadar sağlamdır ki, bugüne kadar bilim adamları bu bariyeri aşan bir ilaç geliştirmeyi başaramamıştı.
 Çalışmanın araştırmacılarından olan Cornell Üniversitesi Veteriner Hekimliği Fakültesi İmmünoloji Anabilim Dalı Öğretim Üyesi Prof. Dr. Margaret Bynoe, nörolojik hastalıkların tedavisinde en önemli engelin, ilacın beyne ulaşmasını engelleyen mekanizmaların olduğunu belirtti. Çalışma, geçtiğimiz günlerde Journal of Neuroscience’da yayımlandı. Çalışma, Ulusal Sağlık Enstitüleri tarafından finansal olarak desteklendi. İlaç firmalarının yaklaşık 100 yıldır kan-beyin bariyerini aşmanın ve hastaları tedavi etmenin yollarını araştırdığını belirten Prof. Dr. Bynoe, buldukları veriler için patent alarak, ilaçların test edileceği ve klinik öncesi çalışmaların yapılacağı Adenios Inc. adında bir firma kurdular.
Çalışmanın araştırmacılarından olan Cornell Üniversitesi Veteriner Hekimliği Fakültesi İmmünoloji Anabilim Dalı Öğretim Üyesi Prof. Dr. Margaret Bynoe, nörolojik hastalıkların tedavisinde en önemli engelin, ilacın beyne ulaşmasını engelleyen mekanizmaların olduğunu belirtti. Çalışma, geçtiğimiz günlerde Journal of Neuroscience’da yayımlandı. Çalışma, Ulusal Sağlık Enstitüleri tarafından finansal olarak desteklendi. İlaç firmalarının yaklaşık 100 yıldır kan-beyin bariyerini aşmanın ve hastaları tedavi etmenin yollarını araştırdığını belirten Prof. Dr. Bynoe, buldukları veriler için patent alarak, ilaçların test edileceği ve klinik öncesi çalışmaların yapılacağı Adenios Inc. adında bir firma kurdular.
Araştırmacılar, şimdiye kadar reseptörlere bağlanarak ve diğer moleküllere yapışarak, kan-beyin bariyerinin aşılabildiğini, ancak bu işlemler sonucunda ilaçların etkinliğinin kaybedildiğini ifade etti. Adenozin reseptörlerinin kan-beyin bariyerinin aşılmasında daha etkili olduğunu belirten araştırmacılar, yeni geliştirdikleri yöntemle, bariyeri istenildiği zaman açıp kapatacak bir mekanizma geliştirmekte olduklarını ifade etti.
Çalışmanın araştırmacıları dekstranlar ve antikorlar kadar büyük makromolekülleri taşıyabildiklerini ve bariyerin aşılmasında molekülün büyüklüğünün bir önemi olup olmadığını araştırdıklarını belirtti. Araştırmacılar, yaptıkları çalışmada bir anti-beta amiloid antikorunun kan-beyin bariyerini aştığını ve transgenik fare modelinde Alzheimer hastalığına neden olan beta-amiloid plaklara bağlandığını gözlemledi.
Tahrip edici immün hücrelerin bariyeri aşarak hastalıklara neden olmasını önlemek amacıyla, bariyeri açmaktan ziyade daha sıkı kapatmayı amaçlayan araştırmacıların ardından, multipl skleroz tedavisi için de benzer bir çalışma başlatıldı.
Farelerde adenozin reseptörleri için bilinen birçok antagonist olmasına karşın (sinyalizasyonu bloke eden ilaç veya proteinler), ileride yapılacak çalışmalarda bu ilaçların insanlar üzerindeki etkisi kesin olarak belirlenebilecek. Araştırmacılar, kan-beyin bariyerini aşan kanser ilaçları geliştirmeyi ve bariyeri modifiye eden adenozin reseptörlerinin altında yatan fizyolojiyi daha iyi anlamayı hedefliyor.
Çalışmanın verileri ne anlama geliyor:
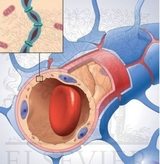 Kan-beyin bariyeri (KBB), merkezi sinir sisteminin (MSS) kapiller mikrovaskülatürü oluşturan özel endotel hücrelerinden oluşmakla birlikte, beyin fonksiyonu için gereklidir. Ayrıca, ilaçların beyne ulaşmasını engellediği için, KBB birçok MSS hastalığının tedavisi önünde büyük bir engel teşkil etmektedir. Bu in vivo çalışmada, adenozin reseptör (AR) sinyalizasyonunun KBB’nin geçirgenliğini modüle ettiği bulundu. Mürin modeli üzerinde yapılan çalışmada, A1 ve A2A AR aktivasyonunun, büyük dekstran ve antikorlardan oluşan makromoleküllerin intravenöz yoldan β-amiloide ulaşmasını kolaylaştırdığı saptandı.
Kan-beyin bariyeri (KBB), merkezi sinir sisteminin (MSS) kapiller mikrovaskülatürü oluşturan özel endotel hücrelerinden oluşmakla birlikte, beyin fonksiyonu için gereklidir. Ayrıca, ilaçların beyne ulaşmasını engellediği için, KBB birçok MSS hastalığının tedavisi önünde büyük bir engel teşkil etmektedir. Bu in vivo çalışmada, adenozin reseptör (AR) sinyalizasyonunun KBB’nin geçirgenliğini modüle ettiği bulundu. Mürin modeli üzerinde yapılan çalışmada, A1 ve A2A AR aktivasyonunun, büyük dekstran ve antikorlardan oluşan makromoleküllerin intravenöz yoldan β-amiloide ulaşmasını kolaylaştırdığı saptandı.
Bununla birlikte, FDA tarafından onaylanan selektif A2A agonist tedavisi Lexiscan da, mürin modellerinde KBB’nin geçirgenliğini artırdı. KBB’nin geçirgenliğinde görülen bu değişiklikler doz bağımlı olup, geçici bir süre için anlamlıydı. A1 veya A2A AR aktivasyonu olmayan transgenik fare modellerinde yapılan çalışmalar ise, AR agonistinin verilmesinin ardından, beyne ulaşan dekstran oranında bir düşüş olduğunu ortaya koydu. Alzheimer hastalığı (AH) olan bir transgenik fare modelinde, geniş spektrumlu AR agonist tedavisini takiben, intravenöz olarak uygulanan anti-β-amiloid antikorunun MSS’ye ulaştığı ve β-amiloid plaklarına bağlandığı gözlemlendi. Selektif AR aktivasyonu in vitro çalışmalarda birtakım hücresel değişikliklere yol açtı. Bunlar transendotelyal elektrik direncinde azalma, aktinomiyosin stres lif oluşumunda artış ve sıkı bağlantı moleküllerinde görülen birtakım değişikliklerdi.
Bu bulgular, ilaçların MSS’ye girişini kolaylaştırmak üzere, in vivo olarak KBB’nin geçirgenliğini modifiye etmek için AR sinyalizasyonunun kullanılabileceğini göstermektedir. Beyin endotel hücrelerindeki AR sinyalizasyonu, KBB’nin geçirgenliğini modifye eden yeni bir endojen mekanizmadır. Bu çalışma bulgularının ilaç tasarımı, ilacın kullanımı ve AH, Parkinson hastalığı, multipl skleroz ve MSS kanserleri gibi nörolojik hastalıklar için tedavi seçeneklerinin geliştirilmesinde katkı sağlayacağını öngörmekteyiz.
KAYNAK: Adenosine Receptor Signaling Modulates Permeability of the Blood–Brain Barrier. Aaron J. Carman, Jeffrey H. Mills, Antje Krenz, Do-Geun Kim, Margaret S. Bynoe. The Journal of Neuroscience, 2011; DOI: 10.1523/JNEUROSCI.3337-11.2011
Çalışmanın tam metnini aşağıdaki linkten okuyabilirsiniz:
http://www.jneurosci.org/content/31/37/13272.abstract
YAZIYI PAYLAŞ


 Alzheimer ve beyin kanserlerinde ilaçlar artık daha etkili olabilecek
Alzheimer ve beyin kanserlerinde ilaçlar artık daha etkili olabilecek Alzheimer’dan korunma ve alınacak yedi basit önlem! Öneriler ve uyarılar…
Alzheimer’dan korunma ve alınacak yedi basit önlem! Öneriler ve uyarılar… Alzheimer nasıl bir hastalıktır? Bol su tüketmek tedaviyi olumlu etkiliyor
Alzheimer nasıl bir hastalıktır? Bol su tüketmek tedaviyi olumlu etkiliyor Zeytinyağı Alzheimer’dan koruyor! Yalnızlık riski arttırıyor
Zeytinyağı Alzheimer’dan koruyor! Yalnızlık riski arttırıyor Alzheimer nedir? Nedenleri, belirtileri, tedavisi ve korunma
Alzheimer nedir? Nedenleri, belirtileri, tedavisi ve korunma Kan-beyin bariyeri bu kez geçici delikler açılarak aşıldı
Kan-beyin bariyeri bu kez geçici delikler açılarak aşıldı
YORUMUNUZ VAR MI?